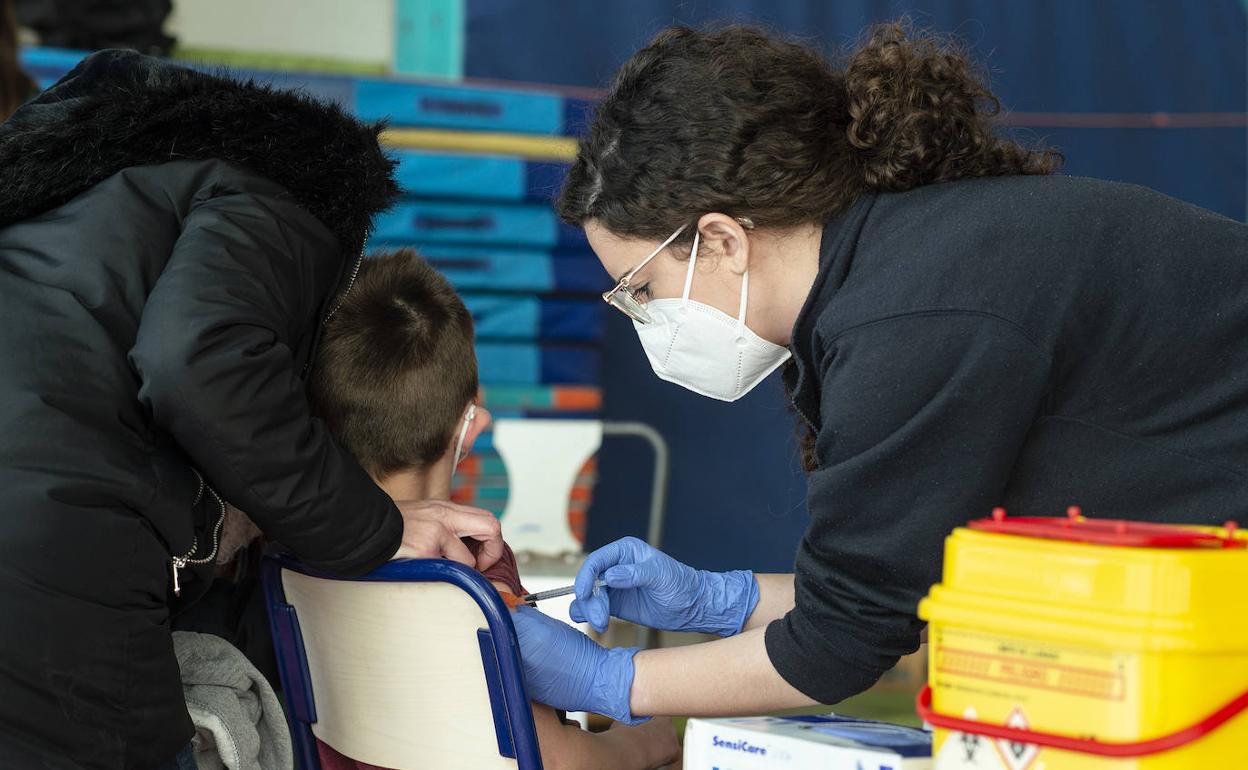
Pfizer pedirá en EE UU la autorización de su vacuna para menores de 5 años
El regulador norteamericano podría aprobarla antes de finales de febrero mientras la empresa estudia administrarla en dos o tres dosis
Pfizer/BioNTech está preparando una petición de autorización para que la FDA, el organismo regular de los medicamentos en Estados Unidos, apruebe su nueva vacuna para niños de entre seis meses y cinco años para uso de emergencia.
Según ha adelantado The Washington Post, esta vacuna para menores de cinco años podría estar disponible a finales de febrero. Sería la primera vacuna disponible en el mundo para ese grupo de edad.
Hasta ahora, la investigación de la vacuna para los más pequeños se ha topado con problemas. Pfizer ha probado con dosis de tres microgramos, una décima del medicamento recibido por los adultos, pero sin los resultados esperados.
En diciembre, la compañía informó de que la inmunización que generaban dos dosis en niños de 2, 3 y 4 años era menor a la que obtenían los adolescentes y los adultos, aunque sí funcionaba en niños de entre 6 meses y dos años. En ese momento, el laboratorio introdujo un tercer pinchazo en el ensayo para mejorar la respuesta inmune.
Si las autoridades sanitarias aprobaran esta vacuna, prácticamente toda la población podría acceder a la inmunización. Desde el 2 de noviembre, Estados Unidos comenzó a administrar la vacuna contra la covid a los niños de entre 5 y 12 años, algo que Europa empezó a hacer a mediados de diciembre tras el visto bueno de la Agencia Europea del Medicamento (EMA, por sus siglas en inglés).